摘要:将循环型电化学氧化中试系统用于对工业高浓度含氨废水的电化学氧化循环处理,研究了循环处理过程中循环液氨氮浓度、pH、浊度、温度、氯离子浓度的变化规律,并计算了处理能耗。实验结果表明,该系统能够通过循环处理使实际废水的氨氮浓度由500mg/L下降至1mg/L以下,提高电流密度是提高系统氨氮去除效率最有效的策略,循环过程中循环液温度和氯离子浓度应保持在合理范围内。该中试系统能够以循环处理的模式高效、稳定、低能耗地处理工业高浓度含氨废水,为更大规模的工业化应用提供了理论依据和实践经验。
关键词:含氨废水;电化学氧化;循环处理;工业应用;中试装置
工业含氨废水具有氨氮浓度高、含盐量高、水量大的特点[1],直接排放至环境会引起富营养化污染,导致水体缺氧并进一步影响水生生物的生长[2-4]。许多工艺被用于工业含氨废水的处理,例如折点氯化法、吹脱法、生物法、化学沉淀法、离子交换法等[5-8]。
相关知识推荐:发表化工论文的期刊
电化学氧化法是一种环境友好型的含氨废水处理技术,具有无二次污染[9-11]、反应条件温和、易于与其他技术联用、处理成本低廉等优点[12-16],近年来受到了科研工作者们的广泛关注,但是基于电化学氧化法的工业应用仍然少有报道。目前的电化学氧化研究多借助槽式反应器,只适合实验室内小规模的废水处理实验[17-19]。李璇[20]报道的连续型电化学反应系统能够大规模处理低氨氮浓度的工业含氨废水,但对于高氨氮浓度的工业废水则需要增大单个电极的极板有效面积或者多级反应器串联,设备成本高昂。本研究在电化学氧化反应器的基础上设计并开发了一套新型中试规模的电化学氧化系统,能够以循环反应模式处理高氨氮浓度的实际工业废水。研究了在循环处理模式下该系统对高氨氮浓度工业废水的处理能力,考察了循环处理过程中循环液氨氮浓度、pH、浊度、温度、氯离子浓度的变化,以期开发一种高效稳定的含氨废水循环处理新工艺。
1实验部分
1.1实验用水
实验所用水样为某燃煤电厂精处理再生废水与氯化钠、氯化铵等药品配制而成,水样水质见表1。
1.2实验装置
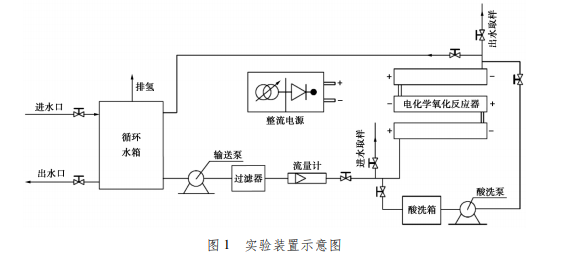
本循环型电化学氧化系统由电化学氧化反应器、过滤器、酸洗系统组成,如图1所示。待处理的废水首先进入循环水箱用药剂调节水质至实验要求。循环处理开始后,循环水首先经过过滤器滤除粒径超过100μm的悬浮物,再经由进水恒流泵输送进入电化学氧化反应器进行氨氮的去除,反应器出水返回至循环水箱。待循环液的氨氮浓度小于1mg/L,循环结束,调节循环水箱中pH合格后外排。电化学氧化反应产物氢气和氮气随出水一起进入循环水箱,再由循环水箱顶部出口进入大气中,防止了易燃易爆气体的集聚。
1.3仪器与分析方法
电化学氧化反应器采用板式双极性电极,阳极为钛基及贵金属氧化物涂层DSA,阴极为大面积纯钛。整个电化学氧化反应器采用三级串联模式,共包含10块极板,极板总有效面积为243.2cm2,其首、末极板与直流电源正、负极相连。电化学氧化反应器有效容积为0.3m3,进水管道和出水管道预留取样口,以方便取样分析进出水水质。
溶液氨氮浓度用水杨酸分光光度法测定,使用美国哈希DR6000紫外可见分光光度计;pH用德国WTWinoLabpH7310酸度计测定;氯离子浓度由瑞士梅特勒SevenCompact离子计测定;温度由德国DITTMER电阻温度计测定;浊度由美国哈希2100Q浊度计测定。
1.4实验方法
采用循环处理模式进行电化学氧化实验。根据实验需求分别控制进水水质、循环时长和反应器电流密度为恒定数值,在电化学氧化反应器进口或出口进行取样,测定水样中的氨氮浓度、浊度、pH、温度、氯离子浓度等,根据测定结果分析变量对电化学氧化过程的影响。实验过程中始终控制反应器出口处水温小于40℃,反应器电流密度小于535mA/cm2,循环液流量大于1.0m3/h。
2结果与讨论
2.1循环处理过程中氨氮去除效率的影响因素
溶液中的氨氮可以通过电化学氧化过程被氧化去除,氧化产物主要为氮气,此外还有少量硝态氮(NO3-)和亚硝态氮(NO2-)[21]。氨氮的电化学氧化过程可分为直接电化学氧化和间接电化学氧化[20]。对于燃煤电厂高氯离子浓度的精处理再生废水主要通过间接电化学氧化过程来去除氨氮,即溶液中的氨氮被反应器阳极产生的强氧化物质,如活性氯(Cl2、HClO、OCl-)、过氧化氢(H2O2)、臭氧(O3)、羟基自由基(·OH)等间接氧化[15]。
以实验用水1(电流密度530mA/cm2)、实验用水1(电流密度220mA/cm2)和实验用水2(电流密度530mA/cm2)分别进行了3次循环电化学氧化处理(循环水量均为1t)。对电化学氧化反应器进口溶液进行取样,分析了电化学氧化系统循环处理对氨氮的去除效率,结果见图2。
如图2所示,在3次循环处理实验中,经过不同的循环反应时长,废水的氨氮浓度最终都小于1mg/L。在相同初始氨氮浓度(500mg/L)条件下,不同电流密度下系统的氨氮去除效率差别显著。在530mA/cm2高电流密度实验条件下,氨氮去除曲线的拟合斜率k值为-197,氨氮去除速率更快;在220mA/cm2低电流密度实验条件下,氨氮去除曲线的拟合斜率k值为-57,氨氮去除速率慢。对于不同初始氨氮浓度(500和250mg/L)的实验废水,保持相同的电流密度(530mA/cm2),氨氮去除曲线的拟合斜率k值(分别为-197和-225)非常接近,氨氮去除速率差别不大。该结果说明,在电化学氧化循环处理模式下,电流密度对氨氮去除效率的影响很大,而初始氨氮浓度的差异对氨氮去除效率的影响可以忽略。在工业化电化学氧化循环处理应用中,可以通过提高电流密度来加快含氨废水的处理速率。
2.2循环液pH变化
在电流密度530mA/cm2条件下,对实验用水2进行了电化学氧化循环处理(循环水量为1t)。对电化学氧化反应器进口溶液进行取样,分析了电化学氧化系统循环处理过程中pH与氨氮浓度的变化关系,结果见图3。
如图3所示,随着电化学氧化循环处理的进行,循环液pH呈先减小后增大的变化趋势。随着循环液氨氮浓度逐渐由250mg/L下降至0,循环液pH也由8.18逐渐降低至2.14。在循环液中的氨氮被完全去除后,继续进行电化学氧化反应,循环液pH由2.14增大至6.38。循环液pH的变化与电化学反应过程有关,当循环液中氨氮未完全反应时,主要发生式(1)的反应生成H+,导致循环液的pH减小;当循环液中的氨氮被完全反应,主要发生式(2)的反应生成OH-,导致循环液的pH增大。在工业化电化学氧化循环处理应用中,氨氮去除过程导致的pH减小能够减弱电化学反应器电极的结垢倾向,从而减少酸洗频率,氨氮完全去除后适当增大循环处理时长又可以调节循环液pH至近中性,从而避免了额外添加药剂调节出水pH。
2.3循环液悬浮物浓度变化
在电流密度530mA/cm2条件下,对实验用水2进行了电化学氧化循环处理(循环水量为1t)。对电化学氧化反应器进口溶液进行取样,分析了电化学氧化系统循环处理过程中循环液浊度的变化规律,结果见图4。
如图4所示,循环液的浊度随着循环电化学氧化处理的进行,由27.2NTU先快速下降至18.2NTU,又逐渐缓慢降低至最低值15.6NTU,最后再回升至26.4NTU。循环液浊度代表了悬浮物数量,在循环反应过程中,悬浮物数量呈现先减少后增多的趋势,该结果与循环液pH变化趋势吻合。由于实验用水2为电厂精处理再生废水,溶液中的铁离子和氧化铁胶体浓度较高,随着循环反应的进行,循环液pH减小使得部分氧化铁胶体反应生成铁离子,循环液浊度减小;当氨氮完全反应后循环液pH增大时,大量铁离子又转化为氧化铁胶体,循环液浊度重新增大。在工业化电化学氧化循环处理应用中,应当在系统中设置过滤系统以保证循环液的浊度始终维持在20NTU以下,使电化学氧化反应器正常运行。
2.4循环液温度变化
在不同环境温度(8和31℃)下,以不同的电流密度对实验用水1进行了电化学氧化循环处理(循环水量为1t)。对电化学氧化反应器出口溶液进行取样,分析了电化学氧化系统循环处理过程中循环液温度的变化,结果见图5。
如图5所示,循环电化学氧化过程中,循环液温度整体呈不断升高的趋势。这是由电极热效率和系统散热性能共同决定的。在相同的电流密度(530mA/cm2)下,环境温度为31℃时循环液从24.5℃升至40.0℃仅需0.9h;而在环境温度为8℃时循环液从24.5℃升至40.0℃需要约4.5h。环境温度相同时(31℃),不同的电流密度(530和220mA/cm2)下,循环液从24.5℃升至40.0℃所需时长分别为0.9和1.1h,升温速率几乎相同。该结果说明,循环实验时的散热效率为影响循环液升温速率的主要因素。循环液温度高于40℃时溶于循环液的HClO和Cl2大量溢出,不利于氨氮氧化反应的发生,将严重影响系统的氨氮去除效率。因此在工业化电化学氧化循环处理应用中应当设置冷却系统以增大系统散热效率,保证即使在环境温度较高的运行条件下,循环液的温度始终低于40℃。
2.5循环液氯离子浓度变化
在电流密度260mA/cm2下,对实验用水3进行了电化学氧化循环处理(循环水量为1t)。对电化学氧化反应器进口溶液进行取样,分析了电化学氧化系统循环处理过程中循环液氯离子浓度的变化规律,结果见图6。
如图6所示,在电化学氧化循环处理过程中,循环液氯离子浓度从2550mg/L持续下降至1750mg/L。在间接电化学氧化过程中,氯离子先反应生成活性氯(Cl2、HOCl、ClO-等),然后再与氨氮进一步反应。其中部分活性氯(Cl2和HOCl)在循环处理过程中从循环水箱溢出至空气中,致使循环液中的氯离子浓度下降。在电化学氧化循环处理工业应用时,应当保持循环水氯离子浓度在2000~8000mg/L范围内,过高的氯离子浓度将使溢出的有效氯增多,增大对环境的污染;过低的氯离子浓度将减弱间接电化学氧化过程,不利于系统对氨氮的去除。
2.6电化学氧化循环处理能耗
如表2所示,不同实验条件下电化学氧化循环处理的能耗不同,在4次典型循环实验中,去除每千克氨氮的能耗在49.3~113.4kW·h范围内。影响能耗的主要因素包括电流密度、循环处理时长、废水水质以及系统中其他设备的能耗。
该结果与王璟等[18]报道的实验室循环降解氨氮平均能耗78~119kW·h/kg较为接近,验证了电化学氧化系统循环处理工业含氨废水中试装置的可行性。
3结论
(1)本实验设计的循环型电化学氧化系统能够以循环模式处理实际工业含氨废水,使不同水质含氨废水的氨氮浓度分别由500和300mg/L达到国家污水综合排放标准(GB8978)中规定的一级排放标准(15mg/L)以下。
(2)电化学氧化反应器电流密度是影响循环处理过程中氨氮去除效率的主要因素,提高电流密度是提高氨氮去除效率最有效的策略。初始氨氮浓度几乎不会影响氨氮去除效率。
(3)在电化学氧化反应第一阶段,循环液的氨氮浓度持续降低,pH逐渐降低,悬浮物浓度不断降低;在电化学氧化反应第二阶段,循环液中的氨氮完全被去除后,pH逐渐增大,悬浮物浓度逐渐增大。整个循环反应过程中,循环液温度不断升高,应始终控制在40℃以下;循环液氯离子浓度持续降低,应始终控制在2000~8000mg/L范围内。
(4)实验中循环处理每千克氨氮的能耗在49.3~113.4kW·h范围内,由多因素共同决定。电化学氧化循环中试实验系统和实验结果为更大规模的工业化应用提供了理论基础和实践经验。——论文作者:徐浩然1*,冯向东1,张贺1,孙伟钢2,吕佳慧3,余一凡3
转载请注明来自:http://www.lunwencheng.com/lunwen/lig/19284.html